⧫25-03-2025⧫
PROPIEDADES DE LOS ALCANOS
Algunos usos de los alcanos
Solubilidad y densidad
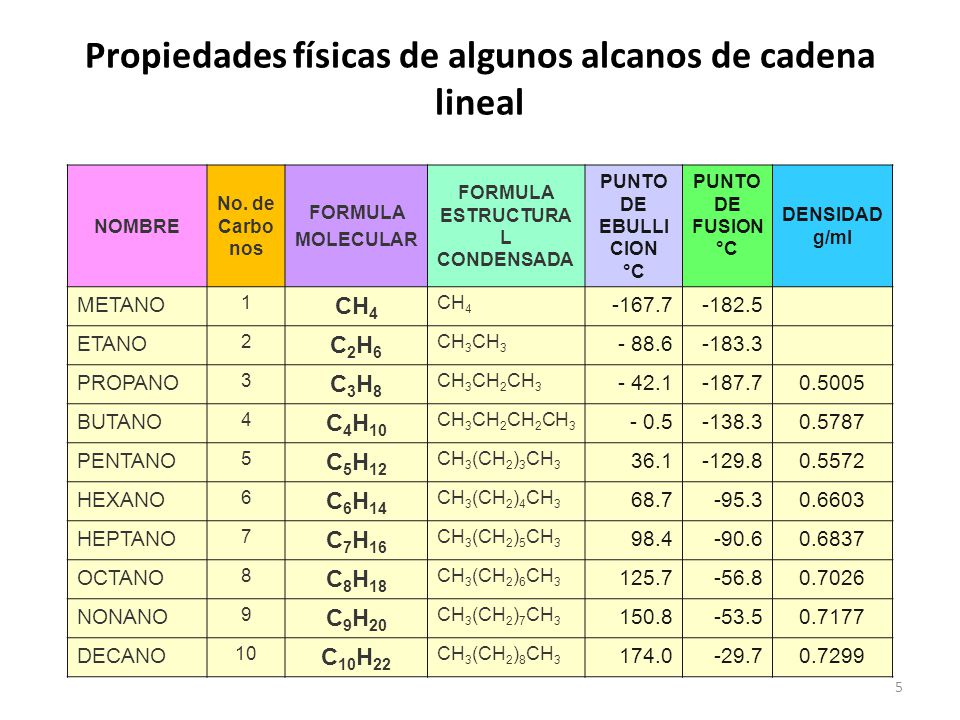
Los alcanos son no polares, lo que los hace insolubles en agua. Sin embargo, son solubles en solventes no polares como otros alcanos. Los alcanos tienen densidades de 0.62 g/mL hasta aproximadamente 0.79 g/mL, que es menos que la densidad del agua (1.0 g/mL).
Lee el siguiente texto...
"Si hay un derrame de petróleo en el océano, los alcanos del petróleo, que no se mezclan con el agua, forman una delgada capa sobre la superficie, que se dispersa sobre un área grande. En abril de 2010, una explosión en una plataforma de perforación en el Golfo de México ocasionó el derrame de petróleo más grande de la historia de Estados Unidos. Todos los días se derramaban aproximadamente 10 millones de litros de petróleo, de abril a julio. Otros grandes derrames de petróleo ocurrieron en Queensland, Australia (2009), la costa de Gales (1996), las islas Shetland (1993) y Alaska, por el Exxon Valdez, en 1989. El petróleo crudo llega a tierra, podría ocasionar un daño muy importante a playas, moluscos, peces, aves y hábitats de vida silvestre. Cuando animales como las aves quedan cubiertos con petróleo, deben limpiarse rápidamente porque la ingestión de hidrocarburos cuando tratan de limpiarse es mortal.
Para la limpieza de los derrames de petróleo se utilizan métodos mecánicos, químicos y microbiológicos. Puede colocarse una barrera flotante alrededor del petróleo que está derramándose para contenerlo hasta que pueda retirarse. Botes llamados espumadoras recogen el petróleo y lo colocan en tanques . Un método químico consiste en utilizar una sustancia para atraer el petróleo, que luego se raspa en tanques de recuperación. Ciertas bacterias que ingieren petróleo se usan para descomponer el petróleo en productos menos dañinos."
Combustión de alcanos
Una reacción de combustión es un cambio químico en el cual un compuesto se combina con oxígeno (O2) para producir calor, luz y productos gaseosos. Por ejemplo, cuando la fuente de O2 es abundante, el metano sufre una combustión completa.