Buenos días mis estudiantes, espero tengan un lindo inicio de semana.
19 de febrero del 2024
Primero vamos a ver el siguiente video para que conozcamos un poco más acerca del carbono, nuestro elemento de estudio durante el grado 11: 💎
Recordemos un poco algunos términos...
Pero para poder que se formen estos tipos de enlace, el carbono tiene que hibridar susorbitales...¿Recuerdas qué es un orbital?Tipos de orbitalesEnlace sigma
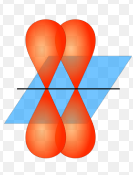
Hibridación de orbitales del carbonoLa configuración electrónica del carbono en su estado natural es:
1s² 2s² 2px¹ 2py¹ 2pz (estado basal)Se ha observado que en los compuestos orgánicos el carbono es tetravalente, es decir, que puede formar 4 enlaces.
Cuando este átomo recibe una excitación externa, uno de los electrones del orbital 2s se excita al orbital 2pz , y se obtiene un estado excitado del átomo de carbono:
1s² 2s¹ 2px¹ 2py¹ 2pz¹ (estado excitado)

.jpg)