Buenos días chicos, cada día es una nueva oportunidad para aprender y superarnos, no temas a los retos porque son el camino hacia el crecimiento. Tengan un bonito día
⧫08-04-2026⧫
Hibridación del Carbono
HIBRIDACIÓN DEL CARBONO
La hibridación del carbono se refiere al proceso mediante el cual los orbitales atómicos del carbono se combinan para formar nuevos orbitales híbridos, que tienen diferentes energías y características geométricas, adaptándose mejor a la formación de enlaces.
En el caso del carbono, existen tres tipos de hibridación más comunes: sp, sp² y sp³, que dependen del número de enlaces que el átomo de carbono forma con otros átomos.
1. Hibridación sp³ (tetraédrica)
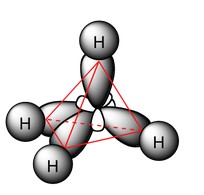
- Ocurre cuando el carbono forma cuatro enlaces sencillos (por ejemplo, en el metano, CH₄).
- Los cuatro orbitales híbridos sp³ se disponen en una geometría tetraédrica, con un ángulo de enlace de aproximadamente 109.5°.
- En esta hibridación, el carbono utiliza un orbital s y tres orbitales p para formar cuatro orbitales híbridos equivalentes, que están orientados hacia los vértices de un tetraedro.
2. Hibridación sp² (trigonal plana)
- Ocurre cuando el carbono forma tres enlaces (por ejemplo, en el eteno, C₂H₄).
- Los tres orbitales híbridos sp² se disponen en una geometría trigonal plana, con un ángulo de enlace de 120°.
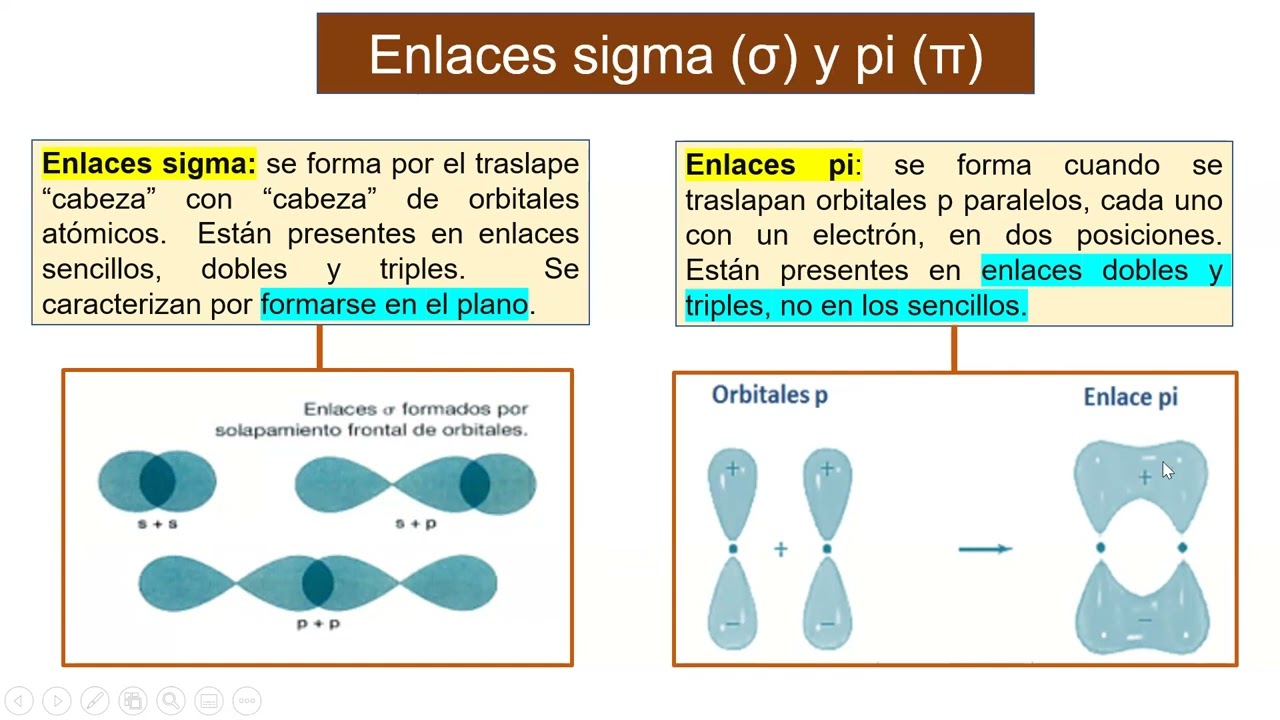
- En esta hibridación, el carbono utiliza un orbital s y dos orbitales p, dejando un orbital p sin hibridar. Este orbital p no hibridado forma un enlace pi (π) con otro orbital p de otro átomo de carbono.
3. Hibridación sp (lineal)
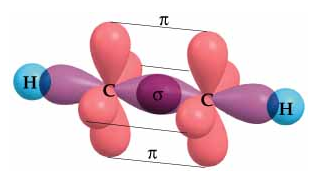
- Ocurre cuando el carbono forma dos enlaces (uno simple y uno triple) con otros átomos.
- El orbital s y un orbital p se combinan para formar dos orbitales híbridos sp, y los otros dos orbitales p quedan sin hibridar para formar enlaces π en el triple enlace.
- Los ángulos de enlace en una molécula con hibridación sp son aproximadamente 180°.
- Ejemplo: el etino (C₂H₂), también conocido como acetileno, donde los dos átomos de carbono están unidos por un triple enlace.