Buenos días niños, cada día es una nueva oportunidad para aprender y superarnos, no temas a los retos porque son el camino hacia el crecimiento. Tengan un bonito día
⧫20-02-2026⧫
2. Hibridación sp² (trigonal plana)
- Ocurre cuando el carbono forma tres enlaces (por ejemplo, en el eteno, C₂H₄).
- Los tres orbitales híbridos sp² se disponen en una geometría trigonal plana, con un ángulo de enlace de 120°.
- En esta hibridación, el carbono utiliza un orbital s y dos orbitales p, dejando un orbital p sin hibridar. Este orbital p no hibridado forma un enlace pi (π) con otro orbital p de otro átomo de carbono.
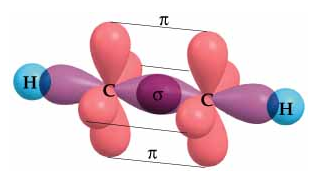
3. Hibridación sp (lineal)
- Ocurre cuando el carbono forma dos enlaces (uno simple y uno triple) con otros átomos.
- El orbital s y un orbital p se combinan para formar dos orbitales híbridos sp, y los otros dos orbitales p quedan sin hibridar para formar enlaces π en el triple enlace.
- Los ángulos de enlace en una molécula con hibridación sp son aproximadamente 180°.
- Ejemplo: el etino (C₂H₂), también conocido como acetileno, donde los dos átomos de carbono están unidos por un triple enlace.
TIPOS DE CARBONO
Se refieren a la cantidad de átomos de carbono a los que está unido un átomo de carbono específico en una molécula.

Ejemplo:
Vamos a dibujar una tabla como la anterior hasta el literal f.
Solución...